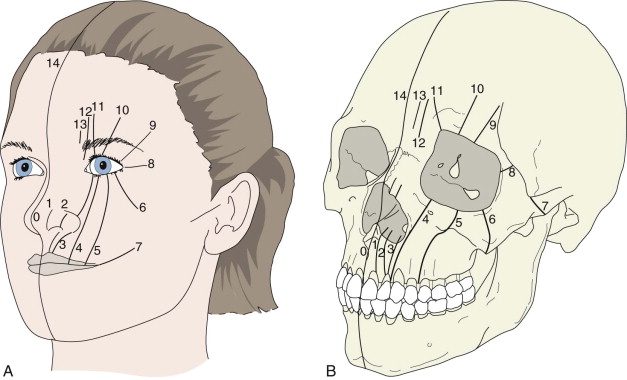
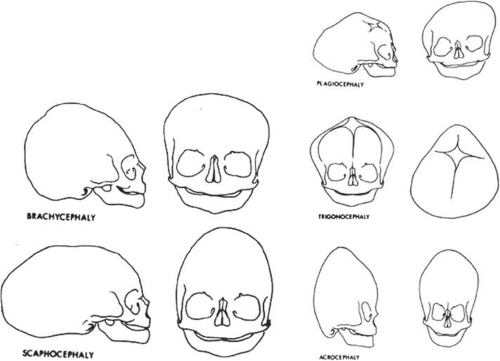
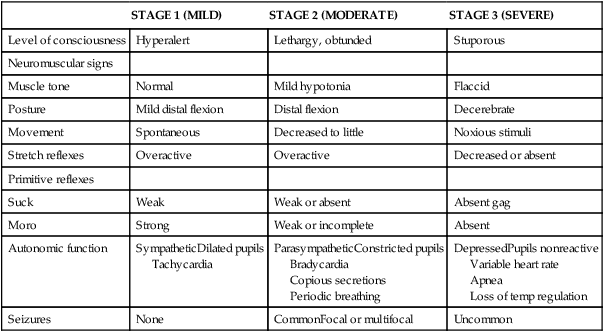
- Técnica de esfigmomanometria: Riva-Rocca 1896.
- Sons de Korotkoff:1913.
- Observou-se que níveis elevados de pressão arterial estavam relacionados a um alto risco de eventos cardiovasculares como: insuficiência cardíaca, encefalopatia, insuficiência renal progressiva, AVC e morte precoce.
- Primeiros anti-hipertensivos: reserpina, hidralazina, clorotiazida.
- Doença cardiovascular crônica mais comum e responsável pela maior parte dos eventos cardiovasculares.
1. Lesão Vascular: lesão endotelial com posterior remodelamento vascular, o qual faz elevar a pressão arterial e esta piora este remodelamento num ciclo vicioso. As consequências deste remodelamento (
1) Arteriosclerose hialina, (2) Arteriosclerose Hiperplásica, (3) Microaneurismas de Charcot-Bouchard, (4) Aterosclerose.
-
Aterosclerose:
O acúmulo de LDL na camada íntima ocorre porque esta pode se ligar a certos proteoglicanos na matriz extracelular, ao se estabelecer na artéria, fica suscetível a sofrer oxidação tanto de sua porção lipídica quanto da proteica. A oxidação no local leve ao aumento da expressão de moléculas de adesão e quimiotáxicas, levando ao acúmulo de leucócitos na íntima junto a gordura. Os monócitos que se fixam na íntima, se transformam em macrófagos, capaz de fagocitar o LDL oxidado - células espumosas. Parte dessas acabam por morrer por apoptose, formando um centro necrótido nas placas mais avançadas.
Lesão inicial da aterosclerose é a chamada estria de gordura que acomete grandes artérias, isso ocorre em todos os indivíduos a partir das primeiras décadas de vida.
A partir ds 30 anos, em pessoas propensas, há evolução para a formada placa de ateroma, progredindo também para artérias de médio calibre (coronárias e carótidas).
A placa de ateroma desenvolve-se preferencialmente nas bifurcações arteriais, onde o turbilhonamento de sangue é maior (ex. bifurcação de carótidas). As porções proximais das artérias de médio calibre também costumam ser afetadas (coronárias, renais, mesentéricas).
O que diferencia a estria gordurosa da placa de ateroma é a presença de
tecido fibroso envolvendo o cerne lipídico. Esse tecido fibroso é produzido por células musculares lisas modificadas que migram da média para a íntima.
Placa de ateroma: tecido fibrolipídico com células no seu interior.
As plaquetas podem aderir a placa - trombo branco - estimulando ainda mais a trombogênese e fibrogênese. Com o passar do tempo, a placa desenvolve microvasos em seu interior, contribuindo para o afluxo de leucócitos e sendo responsável pelos episódios de hemorragia intraplaca.
Fatores de Risco para Aterosclerose: Tabagismo, Obesidade, Sedentarismo, Dislipidemias, HAS, Resistência à insulina, Diabetes mellitus, Hiper-homocisteinemia, PCR aumentada, Microalbuminúria, Idade > 50 anos, Sexo masculino ou sexo feminino pós-menopausa, História Familiar e Infecção pelo HIV.
Papel da Hipertensão Arterial na Aterosclerose: Lesão endotelial + Remodelamento Vascular leva a formação maior de fatores de crescimento e citocinas, maior oxidação de LDL e recrutamento de leucócitos.
Complicações da Placa de Ateroma:
- Obstrução gradual do lúmen arterial - angina estável, angina mesentérica, hipertensão renovascular e claudicação intermitente.
- Fraqueza da parede arterial - Aneurismas.
- Trombose da placa - IAM, AVCi, Isquemia mesentérica aguda - Por que ocorre? Instabilidade da Placa: Leucócitos ativados no interior da placa fagocitam parte da capa fibrótica, esta torna-se fina e se rompe, expondo seu conteúdo lipídico altamente trombogênico às plaquetas e fatores de coagulação, levando a trombose do vaso. Ou seja, há rompimento da placa por conta de uma inflamação da mesma (leucócitos tornam esta fina e frágil).
2. Cardiopatia Hipertensiva:
a. Hipertrofia Ventricular Esquerda:
→ Repercussão cardíaca mais comum da HAS.
→ Massa ventricular esquerda para superfície corporal:
>116 g/m² homens e >96 g/m² mulheres.
→ Presente no ECO de mais de 50% dos Hipertensos não tratados.
→ Em 10% dos ECG de Hipertensos.
→ Fator de risco independente para RCV e mortalidade.
→ Concêntrica ou Excêntrica.
→ Pode haver isquemia miocárdia pelo excesso de demanda metabólica pela hipertrofia, mesmo na ausência de lesão obstrutiva nas coronárias.
 b. Disfunção Diastólica:
b. Disfunção Diastólica:
→ Muito comum ser achado um grau leve de disfunção diastólica ventricular nos hipertensos.
→ Em caso de um grau mais avançado, há aumento do átrio esquerdo e sintomas de congestão pulmonar. (dispneia, ortopneia).
→ Responsável por 50% dos casos de ICC em HAS.
→ Responsável pelo Edema Agudo Hipertensivo.
→ Idosos podem desenvolver
Cardiomiopatia Hipertrófica Hipertensiva: Quadro semelhante à cardiomiopatia hipertrófica hereditária, com HVE concêntrica, com hiperfunção sistólica e disfunção diastólica grave.
c. Cardiopatia Dilatada - Disfunção Sistólica
→ a HAS é a primeira ou segunda causa de Insuficiência Cardíaca no Brasil e no Mundo.
→ disfunção sistólica + dilatação ventricular.
→ inicia-se com IVE e, posteriormente, insuficiência biventricular congestiva.
→ remodelamento cardíaco: cardiopatia dilatada.
→ a diminuição do débito cardíaco pela insuficiência pode
normalizar a PA.
→ mau prognóstico: FE reduzia e/ou NYHA alto.
3. Doença Coronariana:
→ Principal fator de risco para doença aterosclerótica coronariana.
→ Espectro clínico: 1. isquemia silenciosa; 2. angina estável; 3. angina instável; 4. IAM; 5. morte súbita.
→ cardiomiopatia isquêmica pelo miocárdio hibernante pode levar a ICC.
→ IAM pode levar a cardiopatia dilatada e disfunção sistólica.
4. Doença Cerebrovascular:
→ AIT, AVEi, AVEh, HSA, demência multivascular e atrofia cerebral (Doença de Binswanger)
→ O evento cerebrovascular mais comum é o AVEi em 80% dos casos - ocasionado na maioria das vezes por um fenômeno tromboembólico relacionado à aterosclerose carotídea. Outro mecanismo é a trombose in situ dos vasos cerebrais.
→ AIT ocorre por pequenos êmbolos provenientes das carótidas - é um prenuncio do AVCi.
→ Hemorragia intraparenquimatosa ocorre por ruptura de microaneurismas de Charchot-Bouchard.
→ HSA ocorre por ruptura de aneurisma sacular congênito ou MAV.
5. Nefropatia Hipertensiva
→ arteriosclerose hialina nas arteríolas aferentes renais, processo chamado de
nefroesclerose hipertensiva.
→ o primeiro sinal de comprometimento renal é a presença de microalbuminúria: 30-300mg em 24h.
→
microalbuminúria é um fator de risco para morbimortalidade cardiovascular no hipertenso.
→ apenas 0,3% dos hipertensos evoluem com nefropatia.
→ BRASIL – A NH é a primeira causa de rim terminal ( porque os diabéticos morrem antes da fase terminal dos rins) .
Do ponto de vista anátomo-patológico, na nefroesclerose benigna destacam-se alterações vasculares, glomerulares e túbulo-intersticiais. As alterações vasculares caracterizam-se por hialinose arteriolar e arterial, hipertrofia da média e fibrose intimal. As alterações glomerulares nem sempre estão presentes na nefroesclerose benigna. A alteração mais precoce é o colapso das alças capilares, com espessamento aparente de suas paredes, que na verdade decorre do enrugamento da membrana basal glomerular. Outras alterações glomerulares são descritas, por exemplo: aumento da matriz mesangial, que resulta em esclerose segmentar ou global do tufo glomerular. Nefrite intersticial, freqüentemente de intensidade moderada, associa-se às anormalidades vasculares e glomerulares.
Hipertensão Maligna e Anatomopatologia renal: As anormalidades renais incluem rápida elevação de creatinina sérica, hematúria (podendo ser macroscópica), proteinúria, cilindros hemáticos e leucocitários no sedimento. Os níveis plasmáticos de aldosterona promovem alcalose metabólica hipopotassêmica na fase inicial, porém a uremia e a hiperpotassemia podem obscurecer estes achados iniciais. Com freqüência, observam-se sinais hematológicos de anemia hemolítica microangiopática. Do ponto de vista histológico, podem-se observar duas lesões vasculares distintas: a necrose fibrinóide e a arteriolite hiperplásica das arteríolas interlobulares (lesão em “casca de cebola”). Os glomérulos também podem sofrer alterações proliferativas ou necrose, e a maioria das alterações glomerulares e tubulares é secundária a isquemia e ao infarto. A anemia hemolítica microangiopática e a ativação da sistema renina-angiotensina-aldosterona parecem ser essenciais ao seu desencadeamento/perpetuação.
→
Nefroesclerose Hipertensiva Maligna:
- complicação esperada da hipertensão acelerada maligna
- mais comum em negros
- arteríolas renais sofrem um processo de arterioloesclerose hiperplásica e necrose fibrinoide arteriolar.
- Quadro Clínico: Insuficiência renal que progride dias ou semanas + Proteinúria + Hematúria.
- tratar PA corretamente para melhora do quadro renal.
6. Retinopatia Hipertensiva
→ O comprometimento das arteríolas retinianas espelha o acometimento vascular de outros órgãos. (ex. cérebro, rim)
→ Grupos I e II: Efeito do remodelamento vascular = crônico
→ Grupos III e IV: Efeito da hipertensão acelerada maligna
→
Existe correlação entre retinopatia hipertensiva e nefropatia hipertensiva.
Classificação Keith-Wagener-Barker (1939)
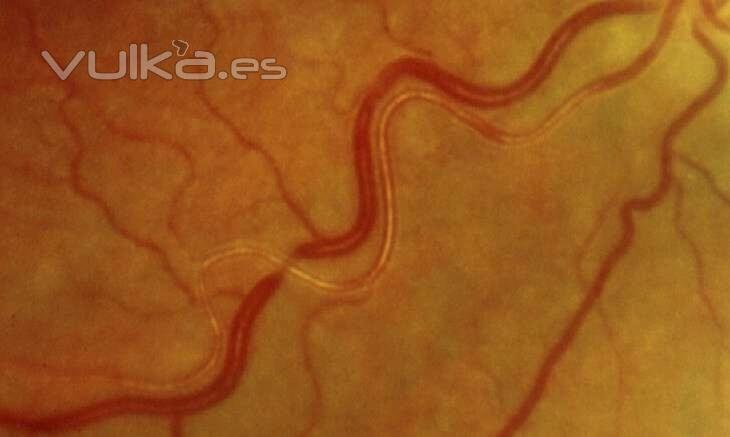 |
| Arteríola em Fio de Prata |
Uma série de manifestações oculares está direta ou indiretamente associada à hipertensão arterial sistêmica (HAS). As consequências diretas incluem retinopatia hipertensiva, coroidopatia e neuropatia óptica. Indiretamente, a HAS é um fator de risco significativo para oclusão venosa e arterial da retina, retinopatia diabética, degeneração macular relacionada à idade e glaucoma. A fundoscopia e o mapeamento de retina com dilatação pupilar devem integrar o exame físico em todos os pacientes com hipertensão recentemente diagnosticada, uma vez que a retina é a única parte da vasculatura que permite visualização de forma não invasiva.
Os sinais de retinopatia hipertensiva podem ser agudos ou crônicos. Os primeiros incluem constrição arteriolar, manchas algodonosas, hemorragias retinianas, exsudatos duros, coroidopatia hipertensiva, descolamento seroso da retina e edema de disco óptico. Cronicamente, há estreitamento arteriolar generalizado, aumento do reflexo dorsal arteriolar, maior tortuosidade vascular, manchas algodonosas e hemorragia retiniana.
Dessa maneira, exames como retinografia, angiofluoresceinografia e tomografia de coerência óptica podem ser indicados para avaliar a perfusão vascular retiniana e a possível necessidade de uso da fotocoagulação a laser ou da injeção intraocular de corticoide e/ou de anti-VEGF. Vale adicionar que não existe tratamento oftalmológico específico para as lesões retinianas causadas pela HAS.
Na gestação, a toxemia gravídica, decorrente da eclâmpsia e da pré-eclâmpsia, pode desencadear estreitamento arteriolar, hemorragia retiniana, exsudatos algodonosos, depósitos lipídicos, edema retiniano e papiledema. Existe ainda a possibilidade de descolamento seroso da retina bilateral em gestantes hipertensas, porém há uma entidade com os mesmos achados denominada coriorretinopatia serosa central. O que a difere da retinopatia hipertensiva é a apresentação unilateral, assim como o bom prognóstico pós-puerpério.
7. Aneurisma de Aorta Abdominal:
→ Geralmente na porção infrarrenal, acomete 3% dos hipertensos.
→ O risco de ruptura se torna importante quando a aorta abdominal mede mais que 5 cm de diâmetro.
8. Claudicação Intermitente: acometimento aterosclerótico de artérias femorais.
-
Identificação de Lesões Subclínicas de Órgãos-alvo:
1. ECG com sinais de HVE
2. ECO com sinais de HVE
3. Espessura médio-intimal de carótida > 0,9mm ou presença de placa de ateroma
4. Índice tornozelo-braquial < 0,9
5. Taxa de Filtração Glomerular < 60 ml/min/1,72m²
6. Microalbuminúria 30-300 mg/24h